Animé par Marc Jaeger, Laboratoire M2P2, Ecole Centrale Marseille
Le 1er juin 2017, 16h30-18h00, amphi de sciences naturelles
C’est sans aucun doute dans les bioprocédés que le rôle de la température est le plus crucial. D’ailleurs la plage de température permettant l’apparition et le maintien de la vie elle-même est ridiculement petite. Une hausse de quelques degrés et c’est tout l’écosystème terrestre qui est chamboulé. Pourtant, alors que nous assistons à une explosion des rapprochements entre biologistes et mathématiciens, physiciens, mécaniciens, chimistes, informaticiens, les thermiciens semblent largement peu touchés par cette tendance ? Alors que biochimie, biophysique, biomécanique font maintenant partie du vocabulaire scientifique, la biothermique reste à inventer. L’objectif de cet atelier est d’abord de susciter l’intérêt puis l’interrogation quant aux raisons de la faible implication de la communauté sur ces problématiques et provoquer ainsi un moment d’échange et de réflexion partagée.
Par le témoignage de trois intervenants nous montrerons que les problèmes de thermiques qui peuvent se poser dans le cadre d’études de biologie ou d’applications biomédicales sont dignes d’intérêt.
Modalités de cryopre?servation pour les formes anciennes et modernes de thérapies cellulaires
Christian Chabannon
Institut Paoli-Calmettes, Inserm CBT-1409, Aix-Marseille Université, F-13273 Marseille
|
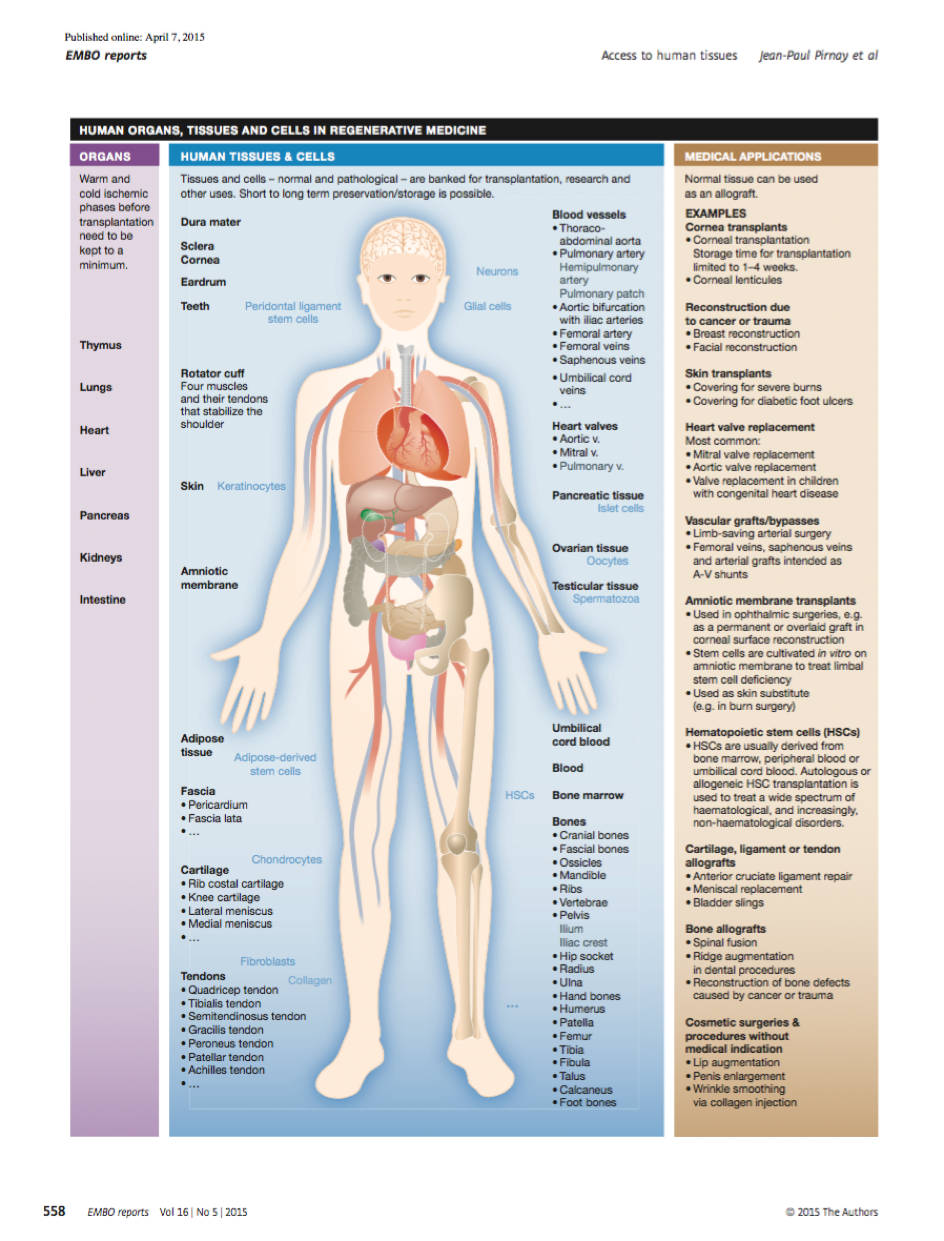
Les thérapies cellulaires modernes émergent historiquement des pratiques de greffes de cellules, tissus et organes. Elles s’en distinguent par la complexité des étapes de transformation des cellules ou tissus primaires avant ré-administration ou réimplantation au malade. Elles s’inscrivent dans un cadre réglementaire récemment défini par les autorités sanitaires Européennes et Américaines en particulier, promouvant une approche de production pharmaceutique centralisée et en conditions aseptiques inspirée du modèle de production du médicament traditionnel. Cette organisation marque une rupture historique avec la pratique des greffes de cellules – dont les greffes de cellules hématopoïétiques sont l’un des rares succès à grandes échelles – et dont la pratique repose sur des réseaux locaux de compétences présents au sein d’établissements de santé : hôpitaux ou établissements de transfusion. Par contraste avec les innovations biologiques, technologiques et logistiques que représente le développement de ces médicaments de thérapies innovantes (MTI), les techniques de cryopréservation essentielles à la bonne préservation de cellules viables pendant les étapes de stockage et de transport ont assez peu évolué ; leur mise en œuvre s’inscrit dans un contexte opérationnel de plus en plus contraint par les aspects réglementaires et normatifs. Des innovations apparaissent cependant sporadiquement, tels que la découverte de nouveaux agents cryoprotecteurs. |
Chabannon C, Sabatier F, Rial-Sebbag E, Calmels B, Veran J, Magalon G, Lemarie C, Mahalatchimy A. “Les unités de Thérapie Cellulaire à l’épreuve de la réglementation sur les médicaments de thérapie innovante“ [Academic cell therapy facilities are challenged by European regulation on advanced therapy medicinal products]. Med Sci (Paris). 2014 May;30(5):576-83. doi: 10.1051/medsci/20143005022. Epub 2014 Jun 13. French. PMID: 24939546
Chabannonc C, Hildebrandt M, Scheding S, Humpe A, Lowdell M, Slaper-Cortenbach I. “Regulation on advanced therapy medicinal products will affect the practice of hematopoietic stem cell transplantation in the near future: a perspective from the EBMT Cell processing committee“, Bone Marrow Transplant. 2015 Mar;50(3):321-3. doi: 10.1038/bmt.2014.271. Epub 2014 Dec 15. No abstract available. PMID: 25501349.
Pirnay JP, Baudoux E, Cornu O, Delforge A, Delloye C, Guns J, Heinen E, Van den Abbeel E, Vanderkelen A, Caroline Van Geyt C, Ivan van Riet I, Gilbert Verbeken G, De Sutter P, Verlinden M, Huys I, Cockbain J, Chabannon C, Dierickx K, Schotsmans P, De Vos D, Rose T, Jennes S, Sterckx S. “Access to human tissues for research and productdevelopment: From EU regulation to alarming legal developments in Belgium", EMBO Rep. 2015 May;16(5):557-62. doi: 10.15252/embr.201540070. Epub 2015 Apr 7. No abstract available. PMID: 25851645.
Svaalgard JD, Haastrup EK, Reckzeh K, Holst B, Glovinski PV, Gørløv JS, Hansen MB, Moench KT, Clausen C, Fischer-Lielsen A. “Low-molecular weight carbohydrate Pentaisomaltose may replace dimethyl sulfoxide as a safer cryoprotectant for cryopreservation of peripheral blood stem cells”, Transfusion, 2016 May;56(5):1088-95. doi: 10.1111/trf.13543. Epub 2016 Mar 15. |
Inverse Heat Transfer Prediction of the freezing front from a cryoprobe
Mohamed Hafid and Marcel Lacroix
Faculté de génie, Université de Sherbrooke, Sherbrooke, Canada
| With the help of a thermocouple inserted into the layer of diseased tissue, the inverse heat transfer method estimates simultaneously the blood perfusion rate and the thermal conductivities of both frozen and unfrozen tissues. This information is then fed to the Pennes bioheat equation that (1) calculates the time-varying temperature distribution inside the layer of tissue and (2) predicts the motion of the freezing front. The effect of the most influential parameters on the inverse predictions is investigated. These parameters are (1) the initial guesses for the unknown Levenberg-Marquardt polynomial parameters of the thermo-physical properties; (2) the temperature of the cryoprobe; (3) the heat transfer coefficient of the impinging jet of liquid nitrogen; and (4) the noise on the temperature data recorded by the thermocouple probe. Results show that the proposed inverse method is a viable alternative to ultrasound and MRI for monitoring the motion of the freezing front during cryosurgery. For all cryogenic scenarios investigated, the predictions of the inverse model remain accurate and stable. |
Thermal biologyat the single cell level
Guillaume Baffou
Institut Fresnel, CNRS, Aix-Marseille Université, Centrale Marseille, F-13013 Marseille
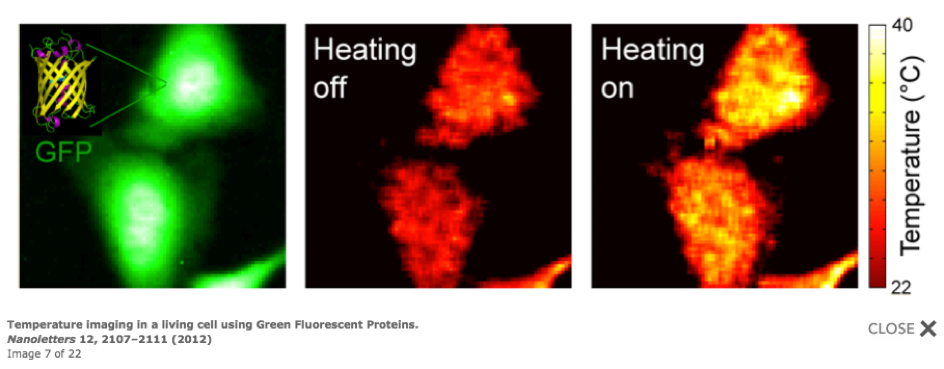
| Le chauffage localisé de cellules uniques par faisceau laser au travers d'un microscope offre de nouvelles perspectives en biologie thermique. Contrairement à l'approche classique qui consiste à étudier l'effet de la température au chauffant tout l'échantillon, voire tout le microscope, l'approche locale permet (i) une dynamique en température bien plus rapide (sub-milliseconde) et (ii) le chauffage de cellules uniques, voire de compartiments cellulaires indépendants. Chauffer des cellules uniques par illumination ne présente pas de difficulté majeure. Le défi consiste plutôt à connaitre le profil de température généré aux petites échelles. Dans cette optique, nous avons récemment développé une technique de microscopie optique capable de cartographier un champ de température avec une résolution de 500 nm et une précision de 1°C. Dans cette présentation, j'expliquerai le principe de fonctionnement de cette technique et je présenterai les applications principales que nous abordons en biologie thermique à l'aide de cette technique, à savoir la croissance de microtubules et le guidage optique de neurones. |
J. Donner, S. Thompson, M. Kreuzer, G. Baffou, R. Quidant, “Mapping intracellular temperature using Green Fluorescent Protein“, Nanoletters 12, 2107-2111 (2012)
M. Zhu, G. Baffou, N. Meyerbröker, and J. Polleux, “Micropatterning Thermoplasmonic Gold Nanoarrays to Manipulate Cell Adhesion“, ACS Nano 6, 7227-7233 (2012)
G. Baffou*, H. Rigneault, D. Marguet, L. Jullien, “A critique of methods for temperature imaging in single cells“, Nature Methods 11, 899-901 (2014)
G. Baffou*, H. Rigneault, D. Marguet, L. Jullien, Reply to: "Validating subcellular thermal changes revealed by fluorescent thermosensors" and "The 10^5 gap issue between calculation and measurement in single-cell thermometry", Nature Methods 12, 803 (2015) |
 |